Abteilung Zell- und Gentherapieentwicklung
Die Abteilung Zell- und Gentherapieentwicklung erforscht und entwickelt zell- und gentherapeutische Technologien und realisiert die Überführung von Herstellungsprozessen aus einem experimentellen Stadium in GMP-konforme Verfahren.
Der Fokus liegt auf antigenspezifischen T-Zellen, CAR-T-Zellen, CAR-NK-Zellen, Dendritischen Zellen, Mesenchymalen Stromazellen und Tissue Engineering Produkten.
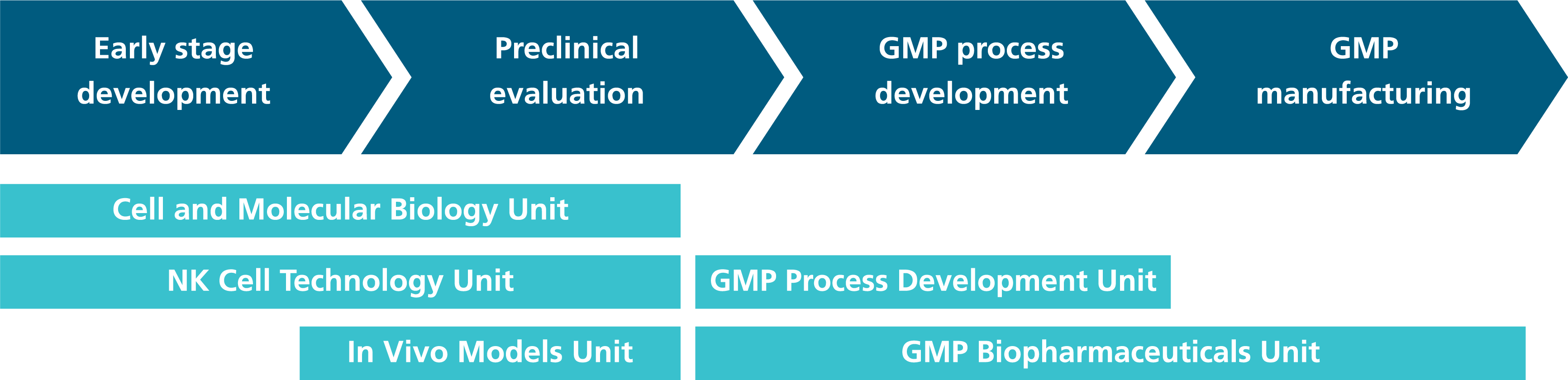
Die aufeinander aufbauenden Kompetenzen der Abteilung umfassen Forschung und Entwicklung, präklinische Evaluierung sowie GMP-Prozessentwicklung für Zell- und Gentherapien bis hin zum Transfer in pharmazeutische Herstellungsprozesse. Dabei können Herstellungsparameter sowie Qualitätskontrollen flexibel und kosteneffizient getestet und optimiert werden.
In allen Entwicklungsstadien werden sowohl neue Technologien (u.a. Digitalisierung, Künstliche Intelligenz, Automatisierung), wie auch klinisch relevante Anwendungsaspekte berücksichtigt.
Darüber hinaus werden in einer eigenen GMP-Herstellungseinheit Biomoleküle wie Antikörper, Proteine, Enzyme und zukünftig auch virale Vektoren in pharmazeutischer Qualität produziert.
Nach erfolgreicher Prozessoptimierung können klinische Prüfmuster durch die Abteilung GMP Zell- und Gentherapie hergestellt und Produkte bis zur Zulassung weiter begleitet werden.